Radioattività e decadimenti nucleari
- P. Strolin
-
Autore della discussione
- Offline
- Premium Utente
-

Less
Di più
11 Anni 9 Mesi fa - 9 Anni 2 Mesi fa #141
da P. Strolin
Con la sua rigorosa metodologia unita a passione e pensiero creativo, la Scienza scopre fenomeni nuovi e del tutto straordinari. Tale è la radioattività, dapprima scoperta come fenomeno naturale e poi utilizzata in numerose applicazioni tra cui la diagnostica medica.
Se pensiamo con mente pronta a volare e non appesantita dall’abitudine, il fenomeno della radioattività può apparire come frutto di magia. Apparente magia, perché è un fenomeno scientificamente fondato in modo rigoroso e non prodotto da fantasia come quanto accade a Harry Potter (figura 1), affascinante in un contesto diverso da quello della realtà fisica. Anzi, doppia apparente magia.
E’ apparente magia la “creazione di materia”: per esempio gli elettroni emessi nei decadimenti beta sono materia apparentemente creata dal nulla. La scoperta della radioattività sfidò il mito del “Nulla si crea, nulla si distrugge”? Esso resisteva dal tempo dei “ filosofi pluralisti ” come Anassagora (circa 496-428 a.C.), Empedocle (circa 492-432 a.C.) e Democrito (circa 460-370 a.C.). Essi ritenevano che la mutevolezza del visibile proviene dalla varietà dei modi secondo cui possono combinarsi degli elementi costituenti intrinsecamente immutevoli: “atomi” per Democrito. Con la Teoria della Relatività la creazione di materia fu poi accettata in una visione allargata della realtà fisica: E = mc 2 permette di trasformare energia in massa, cioè in materia, e viceversa.
E’ apparente magia la “trasmutazione di elementi chimici” associata alla emissione di radiazione. Era il sogno ideale degli alchimisti, che non avrebbero neanche disdegnato poter trasmutare in oro un vil metallo. Nella seconda metà del Settecento, la nascita della Chimica come Scienza moderna portò a considerare immutabili gli elementi chimici e ridusse la passione per l’Alchimia a nicchie marginali. Oltre un secolo dopo, la radioattività naturale mostrò che la realtà fisica può portare a una trasmutazione di elementi chimici: nel decadimento beta un neutrone del nucleo atomico si trasforma in protone o viceversa, e cambia il numero atomico Z che caratterizza gli elementi chimici.
Tutto questo stimola a capire la radioattività come fenomeno fisico. Gli articoli Interazioni Elettro-Deboli (parte iniziale), Nucleo atomico: fenomenologia e Nucleo atomico: legame vanno considerati propedeutici.
Scoperta e prime osservazioni
La fortuna aiuta gli audaci, se come base vi è un lavoro serio e profondo. Nel 1896 Henry Becquerel trovò inspiegabilmente impressionata una lastra fotografica riposta al buio in un cassetto insieme a delle sostanze chimiche contenenti Uranio. Sulla lastra (figura 2) compariva anche l’ombra di una Croce di Malta, che era interposta tra la lastra stessa e i sali di Uranio. Due per due fa quattro: i sali di Uranio emettono una misteriosa “radiazione” e lo spessore della Croce di Malta è sufficiente per assorbirla. L’origine della radiazione sta nel fenomeno che ora chiamiamo “radioattività”.
Fu una scoperta che aprì una nuova era della Fisica. Fino ad allora si conoscevano le leggi classiche della gravitazione e dell'elettromagnetismo. La scoperta della Radioattività fu la fiaccola antesignana di nuove interazioni fondamentali e di nuovi costituenti della materia. A essa, ad esempio, risale la mitica origine della odierna " Interazione Elettro-Debole " e di quanto questa ha portato in termini di conoscenza.
Negli anni dal 1899 al 1903 Ernest Rutherford fece progressi fondamentali per la comprensione del fenomeno osservato da Becquerel. Egli trovò che vi sono tre diversi tipi di radiazioni, caratterizzate da diverse capacità di penetrazione (figura 3). Non potendo dire di più, le chiamò radiazioni α, β e γ. Quest’ultima era stata osservata nel 1900 da Paul Villard come emissione da Radio.
Assieme a Frederick Soddy, Rutherford scoprì anche che la radioattività α e β è accompagnata da una trasmutazione di elemento chimico: il nucleo atomico originario "decade" in un nucleo di massa inferiore.
Le particelle α e i raggi γ sono emesse con un'energia specifica, che dipende dal nucleo che le produce e corrisponde alla differenza di massa tra il nucleo iniziale e quello finale. Le particelle β sono emesse con una distribuzione continua di energia, che va da zero fino al massimo consentito dalla differenza di massa tra nucleo iniziale e finale. Le particelle β si appropriano di solo parte dell'energia disponibile. Nel 1930 l'apparente scomparsa di energia portò Wolfgang Pauli a emettere l’ ipotesi che assieme ad esse viene emesso un neutrino , il quale porta furtivamente via l’energia mancante senza farsi intercettare, perché elettricamente neutro e quindi invisibile ai normali apparati sperimentali.
Nuclei atomici
La figura 4, qui riportata da Nucleo atomico: legame , mostra i nuclei atomici conosciuti in un piano con il numero N di neutroni sull’asse delle ascisse e il numero Z di protoni su quello delle ordinate. Z è il cosiddetto numero atomico e A=N+Z il numero atomico di massa.
In un atomo, il numero di protoni nel nucleo è uguale a quello di elettroni e quindi determina le proprietà dell’elemento chimico corrispondente, rappresentate in modo sistematico nella ben nota “Tavola periodica degli Elementi Chimici”.
Le caratteristiche “radioattive” di un nucleo, cioè il tipo e l’energia delle radiazioni emesse, dipendono invece sia dal numero di protoni che da quello di neutroni e sono quindi diverse per i diversi isotopi di uno stesso elemento chimico.
Nel diagramma in figura 4 i nuclei stabili, cioè quelli che non emettono radiazioni, si situano sulla banda centrale (in nero). Sintetizziamo le considerazioni svolte a questo riguardo nell’articolo sopra citato.
• Protoni e neutroni sono “fermioni” e quindi soggetti al Principio di esclusione di Pauli, come discusso in Lo spin: bosone e fermione? . In assenza di altri effetti, l’energia totale è minima se protoni e neutroni sono in egual numero. Questo spiega la prossimità della banda di stabilità alla linea N=Z.
• L’interazione largamente dominante è l’ Interazione Forte , alla quale si deve la coesione nucleare in dimensioni di cinque ordini di grandezza inferiore a quelle atomiche. Essa fornisce una forza attrattiva, che agisce egualmente su protoni e neutroni, da cui la loro denominazione comune di “nucleoni”. Pur tuttavia, la carica elettrica dei protoni introduce, come effetto minore, una repulsione tra essi. Questo spiega un crescente eccesso di neutroni con l’aumentare della massa del nucleo.
Energia di legame
In Nucleo atomico: legame è illustrato che la massa di un nucleo è eguale alla somma delle masse dei nucleoni liberi meno l’equivalente in massa (secondo E=mc 2 ) dell’energia di legame B. La figura 5 mostra l’energia di legame media per nucleone B/A in funzione del numero atomico di massa A, in milioni di elettron-Volt (MeV). Come detto nel suddetto articolo, l’energia di legame entra con segno negativo nell’espressione dell’energia totale (ossia massa) del nucleo. Quindi al massimo dell’energia di legame per A attorno a 60 corrisponde un minimo dell’energia media per nucleone. Nuclei di massa minore possono fondersi tra loro (processo di “ fusione nucleare ”) e nuclei di massa maggiore possono scindersi (processo di “ fissione nucleare ”), in ambedue i casi con rilascio di energia.
Nuclei instabili e radioattività
I nuclei nella zona gialla attorno alla banda di stabilità sono instabili: essi “decadono”, cioè si trasformano naturalmente in uno di massa inferiore, liberando un’energia corrispondente alla differenza delle loro masse secondo E = mc 2 . L’energia liberata si materializza in particelle (ossia radiazioni) dotate di energia cinetica e quindi capaci di trasferire energia alla materia che incontrano (rivelatori, materia organica o inorganica). In questo consiste la radioattività.
Il momento del decadimento di un nucleo non è prevedibile, ma si può definire un “tempo di dimezzamento” del numero di nuclei iniziali e un “tempo di vita medio” corrispondente, che è il valor medio del tempo di esistenza dei nuclei di una data specie prima del loro decadimento.
Vediamo ora “quali” nuclei decadono e “come” decadono. Mettiamoci negli strettissimi panni dei nuclei, per le varie zone in figura 4.
• Zona gialla sopra la banda di stabilità, per le masse più grandi. I nuclei sono resi instabili dai troppi protoni e hanno anche energeticamente vantaggio a “dimagrire” passando a situazioni con una maggiore energia di legame. Essi emettono un nucleo di 4 He (decadimento α), il nucleo più leggero con N=Z e con forte energia di legame (anche il Deuterio 4 H ha N=Z, ma la sua debole energia di legame lo rende energeticamente sfavorito). A diminuisce di 4 e Z di 2.
• Zona gialla sopra alla banda di stabilità. Il relativo eccesso di protoni è ridotto trasformando un protone in neutrone, con emissione di un positrone (decadimento β + ) e di un neutrino tramite l' Interazione Debole : un “Davide” che mette in riga il “Golia” Interazione Forte e sposta il nucleo verso la linea N=Z.
• Zona gialla sotto la banda di stabilità. Analogamente a quanto detto sopra, il relativo eccesso di neutroni è ridotto trasformando un neutrone in protone, con emissione di un elettrone (decadimento β-) e di un neutrino (più precisamente anti-neutrino).
I suddetti decadimenti implicano un cambiamento di Z e quindi una trasmutazione di elemento chimico, cosa impensabile in fisica classica.
La radioattività γ origina da processi di riassestamento del nucleo verso uno stato di minore energia, senza cambiamenti né di N né di Z. Infatti, dati N e Z, il nucleo puo' esistere in diversi stati quantici e sono possibili transizioni tra questi stati. Non ci si deve stupire: anche la distribuzione degli elettroni nell’atomo può avere diversi stati quantici corrispondenti allo stesso elemento chimico. Gli spettri di emissione (luminosa) atomici costituiscono un fenomeno analogo alla radioattività γ.
In sintesi:
• decadimenti α: Z diminuisce di 2 e A di 4.
• decadimenti β + : Z diminuisce di 1 e A non cambia;
• decadimenti β-: Z aumenta di 1 e A non cambia;
• decadimenti γ: Z e A restano immutati.
I nuclei con massa molto grande sono soggetti a fissione spontanea.
.....
Catena di decadimento dell’Uranio-238
La figura 6 mostra come un nucleo “cammina” nel piano N-Z in seguito a decadimenti β- e α. In particolare, essa mostra la catena di decadimento dell’Uranio-238. Come prodotto intermedio troviamo il Radon-222 (a vita breve), al quale è dedicato un articolo tra i Saggi tematici . Il prodotto finale della catena è il Piombo-206.
.............................................
Fig. 7. Legge esponenziale del decadimento radioattivo in funzione del tempo
Immagine Quark Hochfeiler
Tempo di dimezzamento e legge temporale del decadimento
Una importante proprietà che caratterizza il fenomeno della radioattività è che per ogni radioisotopo esiste un “tempo di dimezzamento” T, pari al tempo necessario affinchè la metà dei nuclei radioattivi iniziali N 0 decada.
Costruiamo la legge temporale del decadimento seguendo la figura 7. Dopo un tempo 2T ne resta la metà della metà, ossia N 0 /4 e così via. Viene in questo modo costruita la legge temporale del decadimento, che corrisponde a un andamento “esponenziale” decrescente. Matematicamente, la legge esponenziale è conseguenza diretta del valore costante della probabilità che un determinato radioisotopo decada in un qualsiasi intervallo di tempo prefissato. Ovviamente, l'esponenziale decresce tanto più rapidamente quanto più piccolo è il tempo di dimezzamento del radioisotopo.
Abbondanze isotopiche naturali
La figura 4 mostra che per un dato numero di protoni Z (ossia elemento chimico) esistono nuclei (detti “isotopi”) con diverso numero di neutroni N e quindi diverso numero atomico di massa A. Le percentuali in massa dei singoli isotopi sono dette “abbondanze isotopiche”.
Si stima che la Terra si è sia formata circa 4,5 miliardi di anni fa con (per ciascun elemento chimico) abbondanze isotopiche primordiali risultanti dai processi che la hanno generata. Le abbondanze degli isotopi instabili sono poi esponenzialmente diminuite in funzione del rapporto (che entra nella potenza con segno negativo) tra il tempo di dimezzamento di ciascun isotopo e l’età della Terra. Sono ancora presenti isotopi instabili primordiali con tempo di dimezzamento confrontabile con l’età della Terra. La combinazione di questi due elementi che determina le attuali abbondanze isotopiche naturali.
Per i più curiosi: una terza apparente magia
Il neutrone libero è instabile e presenta un decadimento β- in protone, elettrone e anti-neutrino, con una vita media di circa 900 secondi nel sistema di riferimento relativistico in cui esso è a riposo. Il protone ha una massa più piccola (seppur di pochissimo) di quella del neutrone ed è quindi preservato dal decadimento β+ in neutrone, elettrone e neutrino.
Se quanto detto sopra accadesse anche per protoni e neutroni all’interno del nucleo, in ogni cosa attorno a noi - e in noi stessi - i nuclei atomici sarebbero presto prosciugati dei loro neutroni a seguito di decadimenti in protoni. Cosa ne ferma l’inesorabile estinzione e evita una totate "protonizzazione"?
Quanto detto sopra sulle masse si riferisce a protoni e neutroni liberi. Per protoni e neutroni nel nucleo si usa la denominazione generica di “nucleoni”, essendo essi molto simili dal punto di vista dell’ Interazione Forte dominante nella coesione nucleare. La usuale metodologia della Fisica Nucleare consiste nel considerare il nucleo come un insieme di nucleoni.
Tuttavia, all'interno di un nucleo il concetto di nucleone è solo il frutto di una pratica ed efficace semplificazione, diciamo pure anche inevitabile salvo casi come quelli discussi in Quarks e gluoni c'era una volta ... . Come discusso in Nucleo atomico: fenomenologia , a stretto rigore si dovrebbe considerare il complesso dei quarks nel nucleo e tutte le loro interazioni.
Invece si tiene conto che i quarks si legano fortemente tre a tre , si assegnano d’ufficio tre quarks in esclusiva a ogni singolo nucleone, si scordano i quarks (confinati nei nucleoni) e i nucleoni vengono indicati come protone o neutrone (la stessa denominazione delle corrispondenti particelle libere) secondo il valore della carica loro elettrica.
Lo si può fare, se si ammette un minimo di elasticità riguardo alle masse. Si deve accettare che le forze residue tra quarks in nucleoni distinti diano loro (attraverso effetti di energie di legame, secondo E=mc 2 ) una sorta di "massa effettiva" diversa da quella che avrebbero come protone o neutrone liberi e indipendenti. All’interno del nucleo viene così energeticamente permesso anche il decadimento β di nucleoni detti protoni in altri detti neutroni: partita pari, senza tempi supplementari e eventuali calci di rigore. Tanto, in ultima analis , al livello fondamentale i decadimenti avvengono tra quarks. Tutto questo, dal punto di vista del nostro istinto di conservazone, ci tranquillizza: non siamo destinati alla protonizzazione.
La radioattività e noi
Abbiamo iniziato con il comprendere la radioattività come fenomeno fisico, facendola uscire dalle nebbie e considerandola nella sua realtà razionale. Altri articoli tra i Saggi tematici trattano del suo impatto sulle nostre conoscenze e sulla nostra vita.
Collegamenti
Renato A. Ricci, Fisica Nucleare , Enciclopedia Treccani (2007)
Radioattività , Laboratorio Nazionale del Gran Sasso, Istituto Nazionale di Fisica Nucleare
La Radioactivité.com , LEDEN e EDP Sciences (in francese e inglese)
The ABC of Nuclear Science , Lawrence Berkeley Laboratory (USA)
Radioactivity , Guide to the Nuclear Wallchart , Contemporary Physics Education Project (CPEP)
Radioactive decay , E=mc 2 explained
.
Professore Emerito di Fisica Sperimentale
Università di Napoli "Federico II"
Complesso Univ. Monte S. Angelo
Via Cintia - 80126 Napoli - Italy
Radioattività e decadimenti nucleari è stato creato da P. Strolin
Radioattività e decadimenti nucleari
..........
................
Per domande: autori o
Domanda a un esperto
................Con la sua rigorosa metodologia unita a passione e pensiero creativo, la Scienza scopre fenomeni nuovi e del tutto straordinari. Tale è la radioattività, dapprima scoperta come fenomeno naturale e poi utilizzata in numerose applicazioni tra cui la diagnostica medica.
Se pensiamo con mente pronta a volare e non appesantita dall’abitudine, il fenomeno della radioattività può apparire come frutto di magia. Apparente magia, perché è un fenomeno scientificamente fondato in modo rigoroso e non prodotto da fantasia come quanto accade a Harry Potter (figura 1), affascinante in un contesto diverso da quello della realtà fisica. Anzi, doppia apparente magia.
| .............................................
Fig. 1. Harry Potter capisce di essere mago
Dal film “Harry Potter e la pietra filosofale (2001); Immagine Buzznet | ... | ......................
Fig. 2. L’inattesa scoperta della radioattività (H. Becquerel,1896)
Immagine Wikipedia |
E’ apparente magia la “creazione di materia”: per esempio gli elettroni emessi nei decadimenti beta sono materia apparentemente creata dal nulla. La scoperta della radioattività sfidò il mito del “Nulla si crea, nulla si distrugge”? Esso resisteva dal tempo dei “ filosofi pluralisti ” come Anassagora (circa 496-428 a.C.), Empedocle (circa 492-432 a.C.) e Democrito (circa 460-370 a.C.). Essi ritenevano che la mutevolezza del visibile proviene dalla varietà dei modi secondo cui possono combinarsi degli elementi costituenti intrinsecamente immutevoli: “atomi” per Democrito. Con la Teoria della Relatività la creazione di materia fu poi accettata in una visione allargata della realtà fisica: E = mc 2 permette di trasformare energia in massa, cioè in materia, e viceversa.
E’ apparente magia la “trasmutazione di elementi chimici” associata alla emissione di radiazione. Era il sogno ideale degli alchimisti, che non avrebbero neanche disdegnato poter trasmutare in oro un vil metallo. Nella seconda metà del Settecento, la nascita della Chimica come Scienza moderna portò a considerare immutabili gli elementi chimici e ridusse la passione per l’Alchimia a nicchie marginali. Oltre un secolo dopo, la radioattività naturale mostrò che la realtà fisica può portare a una trasmutazione di elementi chimici: nel decadimento beta un neutrone del nucleo atomico si trasforma in protone o viceversa, e cambia il numero atomico Z che caratterizza gli elementi chimici.
Tutto questo stimola a capire la radioattività come fenomeno fisico. Gli articoli Interazioni Elettro-Deboli (parte iniziale), Nucleo atomico: fenomenologia e Nucleo atomico: legame vanno considerati propedeutici.
Scoperta e prime osservazioni
La fortuna aiuta gli audaci, se come base vi è un lavoro serio e profondo. Nel 1896 Henry Becquerel trovò inspiegabilmente impressionata una lastra fotografica riposta al buio in un cassetto insieme a delle sostanze chimiche contenenti Uranio. Sulla lastra (figura 2) compariva anche l’ombra di una Croce di Malta, che era interposta tra la lastra stessa e i sali di Uranio. Due per due fa quattro: i sali di Uranio emettono una misteriosa “radiazione” e lo spessore della Croce di Malta è sufficiente per assorbirla. L’origine della radiazione sta nel fenomeno che ora chiamiamo “radioattività”.
Fu una scoperta che aprì una nuova era della Fisica. Fino ad allora si conoscevano le leggi classiche della gravitazione e dell'elettromagnetismo. La scoperta della Radioattività fu la fiaccola antesignana di nuove interazioni fondamentali e di nuovi costituenti della materia. A essa, ad esempio, risale la mitica origine della odierna " Interazione Elettro-Debole " e di quanto questa ha portato in termini di conoscenza.
Negli anni dal 1899 al 1903 Ernest Rutherford fece progressi fondamentali per la comprensione del fenomeno osservato da Becquerel. Egli trovò che vi sono tre diversi tipi di radiazioni, caratterizzate da diverse capacità di penetrazione (figura 3). Non potendo dire di più, le chiamò radiazioni α, β e γ. Quest’ultima era stata osservata nel 1900 da Paul Villard come emissione da Radio.
| .............................................
Fig. 3. Il potere penetrante delle diverse radiazioni; Immagine
INFN - LNGS
| ..... | ...................... La radiazione α è fermata da un foglio di carta. Rutherford dimostrò che le particelle α sono nuclei Elio e più precisamente 4 He. Qualche millimetro di alluminio ferma la maggior parte delle particelle β, successivamente identificate come elettroni (β-) o positroni (ossia anti-elettroni, β + ). Diversi centimetri di un materiale più denso come il piombo sono necessari per assorbire la maggior parte dei raggi γ, i quali sono elettricamente neutri e risultarono essere “ fotoni ”, cioè le particelle corrispondenti alla radiazione elettromagnetica. |
Assieme a Frederick Soddy, Rutherford scoprì anche che la radioattività α e β è accompagnata da una trasmutazione di elemento chimico: il nucleo atomico originario "decade" in un nucleo di massa inferiore.
Le particelle α e i raggi γ sono emesse con un'energia specifica, che dipende dal nucleo che le produce e corrisponde alla differenza di massa tra il nucleo iniziale e quello finale. Le particelle β sono emesse con una distribuzione continua di energia, che va da zero fino al massimo consentito dalla differenza di massa tra nucleo iniziale e finale. Le particelle β si appropriano di solo parte dell'energia disponibile. Nel 1930 l'apparente scomparsa di energia portò Wolfgang Pauli a emettere l’ ipotesi che assieme ad esse viene emesso un neutrino , il quale porta furtivamente via l’energia mancante senza farsi intercettare, perché elettricamente neutro e quindi invisibile ai normali apparati sperimentali.
Fig. 4. La banda di stabilità dei nuclei e le zone instabili
Nuclei atomici
La figura 4, qui riportata da Nucleo atomico: legame , mostra i nuclei atomici conosciuti in un piano con il numero N di neutroni sull’asse delle ascisse e il numero Z di protoni su quello delle ordinate. Z è il cosiddetto numero atomico e A=N+Z il numero atomico di massa.
In un atomo, il numero di protoni nel nucleo è uguale a quello di elettroni e quindi determina le proprietà dell’elemento chimico corrispondente, rappresentate in modo sistematico nella ben nota “Tavola periodica degli Elementi Chimici”.
Le caratteristiche “radioattive” di un nucleo, cioè il tipo e l’energia delle radiazioni emesse, dipendono invece sia dal numero di protoni che da quello di neutroni e sono quindi diverse per i diversi isotopi di uno stesso elemento chimico.
Nel diagramma in figura 4 i nuclei stabili, cioè quelli che non emettono radiazioni, si situano sulla banda centrale (in nero). Sintetizziamo le considerazioni svolte a questo riguardo nell’articolo sopra citato.
• Protoni e neutroni sono “fermioni” e quindi soggetti al Principio di esclusione di Pauli, come discusso in Lo spin: bosone e fermione? . In assenza di altri effetti, l’energia totale è minima se protoni e neutroni sono in egual numero. Questo spiega la prossimità della banda di stabilità alla linea N=Z.
• L’interazione largamente dominante è l’ Interazione Forte , alla quale si deve la coesione nucleare in dimensioni di cinque ordini di grandezza inferiore a quelle atomiche. Essa fornisce una forza attrattiva, che agisce egualmente su protoni e neutroni, da cui la loro denominazione comune di “nucleoni”. Pur tuttavia, la carica elettrica dei protoni introduce, come effetto minore, una repulsione tra essi. Questo spiega un crescente eccesso di neutroni con l’aumentare della massa del nucleo.
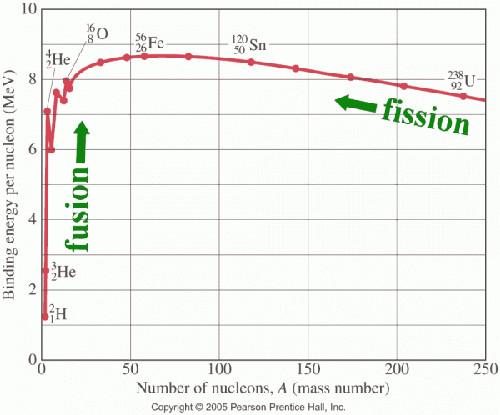
Fig. 5. Energia media di legame per nucleone B/A; Immagine
Science blogs
Energia di legame
In Nucleo atomico: legame è illustrato che la massa di un nucleo è eguale alla somma delle masse dei nucleoni liberi meno l’equivalente in massa (secondo E=mc 2 ) dell’energia di legame B. La figura 5 mostra l’energia di legame media per nucleone B/A in funzione del numero atomico di massa A, in milioni di elettron-Volt (MeV). Come detto nel suddetto articolo, l’energia di legame entra con segno negativo nell’espressione dell’energia totale (ossia massa) del nucleo. Quindi al massimo dell’energia di legame per A attorno a 60 corrisponde un minimo dell’energia media per nucleone. Nuclei di massa minore possono fondersi tra loro (processo di “ fusione nucleare ”) e nuclei di massa maggiore possono scindersi (processo di “ fissione nucleare ”), in ambedue i casi con rilascio di energia.
Nuclei instabili e radioattività
I nuclei nella zona gialla attorno alla banda di stabilità sono instabili: essi “decadono”, cioè si trasformano naturalmente in uno di massa inferiore, liberando un’energia corrispondente alla differenza delle loro masse secondo E = mc 2 . L’energia liberata si materializza in particelle (ossia radiazioni) dotate di energia cinetica e quindi capaci di trasferire energia alla materia che incontrano (rivelatori, materia organica o inorganica). In questo consiste la radioattività.
Il momento del decadimento di un nucleo non è prevedibile, ma si può definire un “tempo di dimezzamento” del numero di nuclei iniziali e un “tempo di vita medio” corrispondente, che è il valor medio del tempo di esistenza dei nuclei di una data specie prima del loro decadimento.
Vediamo ora “quali” nuclei decadono e “come” decadono. Mettiamoci negli strettissimi panni dei nuclei, per le varie zone in figura 4.
• Zona gialla sopra la banda di stabilità, per le masse più grandi. I nuclei sono resi instabili dai troppi protoni e hanno anche energeticamente vantaggio a “dimagrire” passando a situazioni con una maggiore energia di legame. Essi emettono un nucleo di 4 He (decadimento α), il nucleo più leggero con N=Z e con forte energia di legame (anche il Deuterio 4 H ha N=Z, ma la sua debole energia di legame lo rende energeticamente sfavorito). A diminuisce di 4 e Z di 2.
• Zona gialla sopra alla banda di stabilità. Il relativo eccesso di protoni è ridotto trasformando un protone in neutrone, con emissione di un positrone (decadimento β + ) e di un neutrino tramite l' Interazione Debole : un “Davide” che mette in riga il “Golia” Interazione Forte e sposta il nucleo verso la linea N=Z.
• Zona gialla sotto la banda di stabilità. Analogamente a quanto detto sopra, il relativo eccesso di neutroni è ridotto trasformando un neutrone in protone, con emissione di un elettrone (decadimento β-) e di un neutrino (più precisamente anti-neutrino).
I suddetti decadimenti implicano un cambiamento di Z e quindi una trasmutazione di elemento chimico, cosa impensabile in fisica classica.
La radioattività γ origina da processi di riassestamento del nucleo verso uno stato di minore energia, senza cambiamenti né di N né di Z. Infatti, dati N e Z, il nucleo puo' esistere in diversi stati quantici e sono possibili transizioni tra questi stati. Non ci si deve stupire: anche la distribuzione degli elettroni nell’atomo può avere diversi stati quantici corrispondenti allo stesso elemento chimico. Gli spettri di emissione (luminosa) atomici costituiscono un fenomeno analogo alla radioattività γ.
In sintesi:
• decadimenti α: Z diminuisce di 2 e A di 4.
• decadimenti β + : Z diminuisce di 1 e A non cambia;
• decadimenti β-: Z aumenta di 1 e A non cambia;
• decadimenti γ: Z e A restano immutati.
I nuclei con massa molto grande sono soggetti a fissione spontanea.
.....
Fig. 6. Catena di decadimenti dell’Uranio-238; Immagine
Istituto Superiore di Sanità
Catena di decadimento dell’Uranio-238
La figura 6 mostra come un nucleo “cammina” nel piano N-Z in seguito a decadimenti β- e α. In particolare, essa mostra la catena di decadimento dell’Uranio-238. Come prodotto intermedio troviamo il Radon-222 (a vita breve), al quale è dedicato un articolo tra i Saggi tematici . Il prodotto finale della catena è il Piombo-206.
.............................................
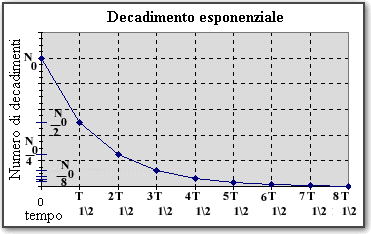
Fig. 7. Legge esponenziale del decadimento radioattivo in funzione del tempo
Immagine Quark Hochfeiler
Tempo di dimezzamento e legge temporale del decadimento
Una importante proprietà che caratterizza il fenomeno della radioattività è che per ogni radioisotopo esiste un “tempo di dimezzamento” T, pari al tempo necessario affinchè la metà dei nuclei radioattivi iniziali N 0 decada.
Costruiamo la legge temporale del decadimento seguendo la figura 7. Dopo un tempo 2T ne resta la metà della metà, ossia N 0 /4 e così via. Viene in questo modo costruita la legge temporale del decadimento, che corrisponde a un andamento “esponenziale” decrescente. Matematicamente, la legge esponenziale è conseguenza diretta del valore costante della probabilità che un determinato radioisotopo decada in un qualsiasi intervallo di tempo prefissato. Ovviamente, l'esponenziale decresce tanto più rapidamente quanto più piccolo è il tempo di dimezzamento del radioisotopo.
Abbondanze isotopiche naturali
La figura 4 mostra che per un dato numero di protoni Z (ossia elemento chimico) esistono nuclei (detti “isotopi”) con diverso numero di neutroni N e quindi diverso numero atomico di massa A. Le percentuali in massa dei singoli isotopi sono dette “abbondanze isotopiche”.
Si stima che la Terra si è sia formata circa 4,5 miliardi di anni fa con (per ciascun elemento chimico) abbondanze isotopiche primordiali risultanti dai processi che la hanno generata. Le abbondanze degli isotopi instabili sono poi esponenzialmente diminuite in funzione del rapporto (che entra nella potenza con segno negativo) tra il tempo di dimezzamento di ciascun isotopo e l’età della Terra. Sono ancora presenti isotopi instabili primordiali con tempo di dimezzamento confrontabile con l’età della Terra. La combinazione di questi due elementi che determina le attuali abbondanze isotopiche naturali.
Per i più curiosi: una terza apparente magia
Il neutrone libero è instabile e presenta un decadimento β- in protone, elettrone e anti-neutrino, con una vita media di circa 900 secondi nel sistema di riferimento relativistico in cui esso è a riposo. Il protone ha una massa più piccola (seppur di pochissimo) di quella del neutrone ed è quindi preservato dal decadimento β+ in neutrone, elettrone e neutrino.
Se quanto detto sopra accadesse anche per protoni e neutroni all’interno del nucleo, in ogni cosa attorno a noi - e in noi stessi - i nuclei atomici sarebbero presto prosciugati dei loro neutroni a seguito di decadimenti in protoni. Cosa ne ferma l’inesorabile estinzione e evita una totate "protonizzazione"?
Quanto detto sopra sulle masse si riferisce a protoni e neutroni liberi. Per protoni e neutroni nel nucleo si usa la denominazione generica di “nucleoni”, essendo essi molto simili dal punto di vista dell’ Interazione Forte dominante nella coesione nucleare. La usuale metodologia della Fisica Nucleare consiste nel considerare il nucleo come un insieme di nucleoni.
Tuttavia, all'interno di un nucleo il concetto di nucleone è solo il frutto di una pratica ed efficace semplificazione, diciamo pure anche inevitabile salvo casi come quelli discussi in Quarks e gluoni c'era una volta ... . Come discusso in Nucleo atomico: fenomenologia , a stretto rigore si dovrebbe considerare il complesso dei quarks nel nucleo e tutte le loro interazioni.
Invece si tiene conto che i quarks si legano fortemente tre a tre , si assegnano d’ufficio tre quarks in esclusiva a ogni singolo nucleone, si scordano i quarks (confinati nei nucleoni) e i nucleoni vengono indicati come protone o neutrone (la stessa denominazione delle corrispondenti particelle libere) secondo il valore della carica loro elettrica.
Lo si può fare, se si ammette un minimo di elasticità riguardo alle masse. Si deve accettare che le forze residue tra quarks in nucleoni distinti diano loro (attraverso effetti di energie di legame, secondo E=mc 2 ) una sorta di "massa effettiva" diversa da quella che avrebbero come protone o neutrone liberi e indipendenti. All’interno del nucleo viene così energeticamente permesso anche il decadimento β di nucleoni detti protoni in altri detti neutroni: partita pari, senza tempi supplementari e eventuali calci di rigore. Tanto, in ultima analis , al livello fondamentale i decadimenti avvengono tra quarks. Tutto questo, dal punto di vista del nostro istinto di conservazone, ci tranquillizza: non siamo destinati alla protonizzazione.
La radioattività e noi
Abbiamo iniziato con il comprendere la radioattività come fenomeno fisico, facendola uscire dalle nebbie e considerandola nella sua realtà razionale. Altri articoli tra i Saggi tematici trattano del suo impatto sulle nostre conoscenze e sulla nostra vita.
Collegamenti
Renato A. Ricci, Fisica Nucleare , Enciclopedia Treccani (2007)
Radioattività , Laboratorio Nazionale del Gran Sasso, Istituto Nazionale di Fisica Nucleare
La Radioactivité.com , LEDEN e EDP Sciences (in francese e inglese)
The ABC of Nuclear Science , Lawrence Berkeley Laboratory (USA)
Radioactivity , Guide to the Nuclear Wallchart , Contemporary Physics Education Project (CPEP)
Radioactive decay , E=mc 2 explained
Vincenzo Roca e Paolo Strolin
.
Professore Emerito di Fisica Sperimentale
Università di Napoli "Federico II"
Complesso Univ. Monte S. Angelo
Via Cintia - 80126 Napoli - Italy
Ultima Modifica 9 Anni 2 Mesi fa da Paolo.
Si prega Accesso a partecipare alla conversazione.
Tempo creazione pagina: 0.577 secondi