- Messaggi: 3
- Ringraziamenti ricevuti 0
Asimmetrie: La chiralità in Chimica
- G. Avitabile
-
Autore della discussione
- Offline
- Nuovo Utente
-

Less
Di più
12 Anni 6 Mesi fa - 9 Anni 2 Mesi fa #106
da G. Avitabile
Questo è parte di una serie di articoli sulle Asimmetrie, che è accompagnata da una analoga sulle Simmetrie. La serie sulle Asimmetrie è delineata in Asimmetrie al grandangolare , ove sono anche esposti gli essenziali concetti propedeutici.
Nell'articolo Asimmetrie: la chiralità negli organismi viventi abbiamo visto che un oggetto è "chirale" quando non è identico alla sua immagine speculare. Un semplice esempio è dato dalle mani, perché la mano destra e la sinistra sono l'immagine speculare l'una dell'altra, ma non sono identiche, come è evidente quando ci infiliamo un guanto.
La chiralità si ritrova anche nel mondo microscopico delle molecole, come vedremo adesso.
Quando un numero limitato di atomi si associano tra di loro con forti legami, mentre formano con gli atomi circostanti solo legami più deboli, costituiscono una molecola. Le dimensioni delle molecole sono di poco superiori a quelle degli atomi, quindi esse sono invisibili a occhio nudo, e anche al microscopio. Il salto di ordini di grandezza dagli oggetti visibili, come le mani o le viti, alle molecole, è da lunghezze dell'ordine di 10 -2 m (centimetri) a lunghezze dell'ordine di 10 -9 m (nanometri), cioè un fattore di circa 10 7 (dieci milioni).
Molte molecole sono chirali. Il caso più comune è quello di un atomo di carbonio legato a 4 sostituenti diversi. Vediamo più in dettaglio.
Le proteine sono fra le molecole più importanti per la vita. Sono catene costituite dalla successione di amminoacidi, che possono essere di 20 tipi diversi. La figura 2 mostra la struttura di uno di questi amminoacidi. Intorno al C centrale abbiamo 4 sostituenti diversi: un H come nel metano, un gruppo -COOH, un gruppo -NH 2 e un gruppo indicato genericamente come -R, che può essere di 20 tipi diversi e definisce di quale dei 20 amminoacidi naturali si tratta.
Questa molecola è chirale, ossia esistono 2 molecole diverse (per un dato -R), rappresentate una nella mano destra e l'altra nella sinistra, e dette "enantiomeri".
E' interessante notare che i 20 amminoacidi naturali hanno tutti la configurazione indicata a sinistra nella figura, che è detta configurazione L. La configurazione indicata nella mano destra è detta D e non si trova normalmente in natura, tranne in casi eccezionali in alcuni batteri.
Nomenclatura degli enantiomeri
I termini L e D hanno origine dalla proprietà delle sostanze chirali di ruotare il piano di vibrazione di un raggio di luce polarizzata che le attraversi. I due enantiomeri ruotano questo piano, come è richiesto dalla relazione di simmetria tra di loro, della stessa quantità in valore assoluto ma in direzioni opposte: a quello che lo ruota verso destra fu assegnata la denominazione D, a quello verso sinistra il nome L.
In seguito però la convenzione fu cambiata. Infatti la direzione in cui ruota la luce polarizzata non è un fattore importante per molti aspetti, e non è legata in modo semplice alla struttura, per cui è imprevedibile e si determina solo sperimentalmente. Più importante, per comprendere molti meccanismi chimici, è la configurazione assoluta, quella descritta nella figura 2. Fra gli amminoacidi naturali, molti ruotano la luce verso sinistra, ed erano designati L. Allora si decise di designarli L tutti e 20 (anzi 19, perché uno non è chirale), anche quelli che ruotano il piano della luce verso destra. In questo modo i simboli L e D indicano la configurazione assoluta e non necessariamente il verso di rotazione. Per considerazioni analoghe, tutti gli zuccheri naturali sono designati D.
A complicare ancora la questione della nomenclatura, si deve notare che il metodo ora descritto si applica facilmente a una serie di composti simili come gli amminoacidi, ma non si estende facilmente a composti diversi. Per questo è stato formulato un sistema ufficiale diverso, che assegna la configurazione chirale a qualsiasi molecola in base alla sola geometria della molecola, e usa nomi diversi: R o S. I biochimici preferiscono ancora il sistema D-L, quindi la situazione dei nomi resta confusa.
Somiglianze e differenze fra enantiomeri
Due enantiomeri, cioè due molecole che sono l'una l'immagine speculare dell'altra, sono, come le mani, uguali ma non sovrapponibili e presentano somiglianze e differenze con modalità particolari. I due enantiomeri sono identici riguardo a tutte le proprietà che non risentono della riflessione in uno specchio: la massa, le dimensioni, il colore (che per le molecole significa lo spettro di assorbimento nella luce visibile, ma l'uguaglianza si estende all'infrarosso e all'ultravioletto). Sono identici anche nelle reazioni con altre molecole non chirali. Le differenze sorgono, e possono essere importantissime, quando i due enantiomeri interagiscono con altre molecole chirali.
Interazioni di enantiomeri con altre molecole chirali
Fate il confronto con le due mani: anche loro hanno la stessa massa, grandezza, colore, capacità di infilarsi un anello (oggetto non chirale). Ma se infilate un guanto, la mano destra vuole il guanto destro e rifiuta il sinistro. Questo però significa che la mano sinistra a sua volta vuole il guanto sinistro (l'enantiomero del guanto destro) e rifiuta il destro.
Se invece una sostanza chirale A, costituita dagli enantiomeri A L e A D , reagisce con una sostanza chirale B, costituita da enantiomeri B L e B D , le possibilità sono più numerose. A L vedrà B L e B D come due molecole diverse, e reagirà con loro con facilità diversa (come la mano destra infila con facilità diversa il guanto destro e il guanto sinistro). Se A L può reagire con B L , allora A D può reagire nello stesso modo con B D , producendo A D B D , enantiomero di A L B L . Analogamente, se A L può reagire con B D dando A L B D , allora A D reagisce con la stessa facilità con B L , producendo A D B L .
E se due molecole non chirali A e B reagiscono, possono dare un prodotto chirale AB? Sì, ma per simmetria produrranno la stessa quantità dei due enantioneri (AB) L e (AB) D , perché non hanno ragione di preferire l'uno all'altro.
In conclusione, se nelle molecole dei reagenti non c'è chiralità essa o non si crea o si producono in misura uguale i due enantiomeri. Ma se nelle molecole dei reagenti c'è chiralità, questa si può mantenere o anche estendere nella reazione. Vedremo in conclusione cha questa considerazione ha conseguenze molto importanti.
Molecole chirali nei viventi
Molecole chirali sono diffuse in tutti gli esseri viventi e sono essenziali per la vita. Oltre agli amminoacidi, sono chirali tutti gli zuccheri. Anche i diversi zuccheri, come gli amminoacidi, hanno tutti la stessa configurazione, ma la situazione è più complicata per la presenza di diversi centri chirali in ciascuna molecola. Mentre gli amminoacidi hanno configurazione L, gli zuccheri hanno quasi tutti configurazione D.
Il fatto poi che tutti i viventi presentano la stessa scelta, è uno dei tanti indizi che la vita sulla Terra è un fenomeno unitario, e che tutti gli esseri viventi derivano da un'unica origine, qualunque essa sia.
Professore di Chimica macromolecolare (in pensione)
Universita' degli Studi Federico II di Napoli
Asimmetrie: La chiralità in Chimica è stato creato da G. Avitabile
Asimmetrie: la Chiralità in Chimica
e l'asimmetria chimica dei viventi
......................
................
e l'asimmetria chimica dei viventi
Per domande: autore o
Domanda a un esperto
................Questo è parte di una serie di articoli sulle Asimmetrie, che è accompagnata da una analoga sulle Simmetrie. La serie sulle Asimmetrie è delineata in Asimmetrie al grandangolare , ove sono anche esposti gli essenziali concetti propedeutici.
Nell'articolo Asimmetrie: la chiralità negli organismi viventi abbiamo visto che un oggetto è "chirale" quando non è identico alla sua immagine speculare. Un semplice esempio è dato dalle mani, perché la mano destra e la sinistra sono l'immagine speculare l'una dell'altra, ma non sono identiche, come è evidente quando ci infiliamo un guanto.
La chiralità si ritrova anche nel mondo microscopico delle molecole, come vedremo adesso.
La Chiralità in Chimica
Quando un numero limitato di atomi si associano tra di loro con forti legami, mentre formano con gli atomi circostanti solo legami più deboli, costituiscono una molecola. Le dimensioni delle molecole sono di poco superiori a quelle degli atomi, quindi esse sono invisibili a occhio nudo, e anche al microscopio. Il salto di ordini di grandezza dagli oggetti visibili, come le mani o le viti, alle molecole, è da lunghezze dell'ordine di 10 -2 m (centimetri) a lunghezze dell'ordine di 10 -9 m (nanometri), cioè un fattore di circa 10 7 (dieci milioni).
Molte molecole sono chirali. Il caso più comune è quello di un atomo di carbonio legato a 4 sostituenti diversi. Vediamo più in dettaglio.
| .............................................
Fig. 1. Molecola di metano | .... | ............................................................................ L'atomo di carbonio può formare 4 legami. Quando ciò avviene, i legami sono diretti verso i 4 vertici di un tetraedro, come in figura 1, che rappresenta una molecola di metano, CH 4 . La pallina nera al centro rappresenta un atomo di carbonio C, le palline più chiare gli atomi di idrogeno H. Nel metano i 4 atomi H sono indistinguibili perché equivalenti per simmetria: se ruotiamo la molecola mettendo un H al posto di un altro, la situazione finale sarà identica a quella iniziale. Ma se i 4 sostituenti, invece di essere uguali come gli H nel metano, sono tutti diversi tra di loro, la molecola risulta chirale, cioè non sovrapponibile alla sua immagine speculare. |
Le proteine sono fra le molecole più importanti per la vita. Sono catene costituite dalla successione di amminoacidi, che possono essere di 20 tipi diversi. La figura 2 mostra la struttura di uno di questi amminoacidi. Intorno al C centrale abbiamo 4 sostituenti diversi: un H come nel metano, un gruppo -COOH, un gruppo -NH 2 e un gruppo indicato genericamente come -R, che può essere di 20 tipi diversi e definisce di quale dei 20 amminoacidi naturali si tratta.
Questa molecola è chirale, ossia esistono 2 molecole diverse (per un dato -R), rappresentate una nella mano destra e l'altra nella sinistra, e dette "enantiomeri".
| ......................................................................... Fig. 2. Amminoacidi L (a sinistra) e D (a destra) Immagine Physical Methods in Chemistry and Nano Science | .... | ............................................................................................... I due enantiomeri non sono sovrapponibili. Infatti nella molecola rappresentata in figura 2 nella mano sinistra abbiamo H a sinistra e R a destra. Se la ruotiamo per mettere R a sinistra e H a destra (come nella molecola nella mano destra), porteremo il gruppo -NH 2 in avanti e non all'indietro, come è in tutte e due le molecole disegnate; oppure per lasciare -NH 2 all'indietro, dovremmo metterlo in alto e non in basso, scambiandolo con -COOH. Insomma, per quanto ruotiamo uno dei due enantiomeri, non lo sovrapporremo mai all'altro, proprio come muovendo una mano, non la sovrapponiamo mai all'altra. Una presentazione della chiralità molecolare si può trovare anche nella pagina dal titolo Enantiomeri su What is chemistry? . |
E' interessante notare che i 20 amminoacidi naturali hanno tutti la configurazione indicata a sinistra nella figura, che è detta configurazione L. La configurazione indicata nella mano destra è detta D e non si trova normalmente in natura, tranne in casi eccezionali in alcuni batteri.
Nomenclatura degli enantiomeri
I termini L e D hanno origine dalla proprietà delle sostanze chirali di ruotare il piano di vibrazione di un raggio di luce polarizzata che le attraversi. I due enantiomeri ruotano questo piano, come è richiesto dalla relazione di simmetria tra di loro, della stessa quantità in valore assoluto ma in direzioni opposte: a quello che lo ruota verso destra fu assegnata la denominazione D, a quello verso sinistra il nome L.
In seguito però la convenzione fu cambiata. Infatti la direzione in cui ruota la luce polarizzata non è un fattore importante per molti aspetti, e non è legata in modo semplice alla struttura, per cui è imprevedibile e si determina solo sperimentalmente. Più importante, per comprendere molti meccanismi chimici, è la configurazione assoluta, quella descritta nella figura 2. Fra gli amminoacidi naturali, molti ruotano la luce verso sinistra, ed erano designati L. Allora si decise di designarli L tutti e 20 (anzi 19, perché uno non è chirale), anche quelli che ruotano il piano della luce verso destra. In questo modo i simboli L e D indicano la configurazione assoluta e non necessariamente il verso di rotazione. Per considerazioni analoghe, tutti gli zuccheri naturali sono designati D.
A complicare ancora la questione della nomenclatura, si deve notare che il metodo ora descritto si applica facilmente a una serie di composti simili come gli amminoacidi, ma non si estende facilmente a composti diversi. Per questo è stato formulato un sistema ufficiale diverso, che assegna la configurazione chirale a qualsiasi molecola in base alla sola geometria della molecola, e usa nomi diversi: R o S. I biochimici preferiscono ancora il sistema D-L, quindi la situazione dei nomi resta confusa.
Somiglianze e differenze fra enantiomeri
Due enantiomeri, cioè due molecole che sono l'una l'immagine speculare dell'altra, sono, come le mani, uguali ma non sovrapponibili e presentano somiglianze e differenze con modalità particolari. I due enantiomeri sono identici riguardo a tutte le proprietà che non risentono della riflessione in uno specchio: la massa, le dimensioni, il colore (che per le molecole significa lo spettro di assorbimento nella luce visibile, ma l'uguaglianza si estende all'infrarosso e all'ultravioletto). Sono identici anche nelle reazioni con altre molecole non chirali. Le differenze sorgono, e possono essere importantissime, quando i due enantiomeri interagiscono con altre molecole chirali.
Interazioni di enantiomeri con altre molecole chirali
Fate il confronto con le due mani: anche loro hanno la stessa massa, grandezza, colore, capacità di infilarsi un anello (oggetto non chirale). Ma se infilate un guanto, la mano destra vuole il guanto destro e rifiuta il sinistro. Questo però significa che la mano sinistra a sua volta vuole il guanto sinistro (l'enantiomero del guanto destro) e rifiuta il destro.
| ......................................................................... Fig. 3. Una molecola chirale richiede il ricettore adatto Immagine UC Davis - Chemwiki | ..... | ............................................................................................... Anche una scarpa destra e la sinistra sono due enantiomeri, ma nessuna delle due si infila bene nella mano (destra o sinistra); si infila però nel piede (oggetto chirale), rispettando la chiralità (scarpa destra col piede destro). A livello delle molecole, possiamo dire che una molecola non chirale vede due enantiomeri come due molecole uguali. Una molecola di alcool etilico (non chirale) reagisce indifferentemente con i due enantiomeri di un amminoacido (chirale) dando due prodotti che sono enantiomeri fra di loro (un anello si infila nella mano destra o sinistra dando una mano inanellata, destra o sinistra). Al contrario di questo, una molecola chirale vede due enantiomeri come due molecole diverse. La figura 3 illustra schematicamente come una molecola chirale si leghi solo con il ricettore adatto. |
Se invece una sostanza chirale A, costituita dagli enantiomeri A L e A D , reagisce con una sostanza chirale B, costituita da enantiomeri B L e B D , le possibilità sono più numerose. A L vedrà B L e B D come due molecole diverse, e reagirà con loro con facilità diversa (come la mano destra infila con facilità diversa il guanto destro e il guanto sinistro). Se A L può reagire con B L , allora A D può reagire nello stesso modo con B D , producendo A D B D , enantiomero di A L B L . Analogamente, se A L può reagire con B D dando A L B D , allora A D reagisce con la stessa facilità con B L , producendo A D B L .
E se due molecole non chirali A e B reagiscono, possono dare un prodotto chirale AB? Sì, ma per simmetria produrranno la stessa quantità dei due enantioneri (AB) L e (AB) D , perché non hanno ragione di preferire l'uno all'altro.
In conclusione, se nelle molecole dei reagenti non c'è chiralità essa o non si crea o si producono in misura uguale i due enantiomeri. Ma se nelle molecole dei reagenti c'è chiralità, questa si può mantenere o anche estendere nella reazione. Vedremo in conclusione cha questa considerazione ha conseguenze molto importanti.
Rottura della simmetria negli esseri viventi
Molecole chirali nei viventi
Molecole chirali sono diffuse in tutti gli esseri viventi e sono essenziali per la vita. Oltre agli amminoacidi, sono chirali tutti gli zuccheri. Anche i diversi zuccheri, come gli amminoacidi, hanno tutti la stessa configurazione, ma la situazione è più complicata per la presenza di diversi centri chirali in ciascuna molecola. Mentre gli amminoacidi hanno configurazione L, gli zuccheri hanno quasi tutti configurazione D.
| ................................................................................ La chiralità delle molecole non è solo quella dovuta agli atomi di carbonio asimmetrici: può formarsi anche a livello di strutture più grandi, comprendenti molti atomi. In particolare, le macromolecole biologiche (proteine e acidi nucleici) hanno strutture a lunga catena, e la catena, come un filo, può ripiegarsi in vari modi, dando luogo a strutture diverse. Una delle più comuni è l'avvitamento ad elica, e l'elica è una struttura chirale, cioè l'avvitamento può avvenire in due sensi speculari, proprio come la filettatura di una vite. Struttura delle proteine Le proteine ripiegano la loro catena in maniera ben definita, dando alla molecola una forma precisa, strettamente legata alle diverse funzioni biologiche che le proteine possono avere. Alcuni tratti, generalmente brevi, di una catena proteica, possono avere una struttura ad elica: l'α-elica, scoperta da Linus Pauling nel 1951. L'elica è una struttura chirale. Se le catene fossero simmetriche, i due versi dell'elica sarebbero equivalenti e si formerebbero in quantità uguali; ma nelle proteine la catena proteica, quella che si avvolge ad elica, è essa stessa chirale, e questo rende i due versi dell'elica non equivalenti. Sperimentalmente si è visto che si forma sempre l'elica destra, quella mostrata in figura 4, tratta da G Botelho and O. Lupi, Int. J. Dermatology 2008, 47, 1225-1233. | ...... | ............................
Fig. 4. L'elica α delle proteine Immagine Int. J. Derm. |
| .....................................................................
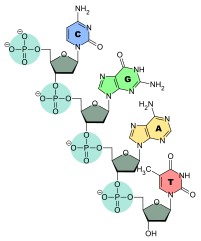
Fig. 5. Formula del DNA - Immagine
Wikipedia
| ..... | .............................................................................................................. ll DNA Negli acidi nucleici, di cui il più noto è il DNA, la struttura ad elica è la norma generale; nel DNA in particolare, si forma la famosa doppia elica, formata da due catene allacciate tra loro e avvolte a elica. Vediamola più in dettaglio (un'altra descrizione si può trovare nella pagina dal titolo L'eredità genetica su What is chemistry? ). La formula del DNA è schematizzata in figura 5. La catena è formata dalla successione di nucleotidi, ognuno formato da 3 elementi: un fosfato (cerchio verde chiaro), uno zucchero (deossiribosio, pentagono verde scuro) e una base (C,G,A,T). I fosfati fanno da ponte fra i vari nucleotidi, essendo legati a due residui di zucchero diversi. La catena è molto più lunga dei 4 nucleotidi disegnati. Il deossiribosio è chirale, sempre nella forma D, e rende chirale tutta la catena; fosfato e zucchero sono uguali in tutti i nucleotidi. La base può essere di 4 tipi diversi, C,G,A,T per cui nel DNA si trovano 4 nucleotidi diversi, che possono stare in qualsiasi sequenza e rendono il DNA di una persona diverso da tutti gli altri. E' questa sequenza di basi che si determina nelle analisi del DNA. |
| .....................................................................
Fig. 6. Le coppie di basi nel DNA
Immagine Base Pairing | ..... | .................................................................................. La doppia elica del DNA La catena del DNA non è singola ma doppia. Infatti ognuna delle 4 basi si lega specificamente con una e una sola altra base, attraverso legami idrogeno, secondo lo schema in figura 6. Una catena singola, che può avere le 4 basi in una sequenza qualsiasi, per es. ...ATTGAC..., deve perciò obbligatoriamente essere legata a un'altra in direzione inversa e con sequenza complementare, nell'es. ...GTCAAT... Questa coppia di catene costituisce il filamento di DNA, che poi si avvolge a doppia elica, ed essendo chirale distingue l'elica destra da quella sinistra. Sono possibili eliche di diversi tipi per il DNA, con avvolgimento destro o sinistro, ma la più comune è quella detta DNA B, una doppia elica destra mostrata in figura 7. Nel DNA come nelle proteine, la formazione di un'elica crea una struttura chirale estesa su una scala molto più grande del singolo carbonio asimmetrico. |
| .. .. L'ambiente vivente è chirale Le strutture viventi sono quindi ambienti altamente chirali, per i quali i due enantiomeri di una qualsiasi molecola chirale sono da considerare molecole diverse. Tornando al paragone con le mani, possiamo paragonare un essere vivente a una scatola di guanti destri. Se ci introduco la mano destra, gli effetti potranno essere ben diversi da quando ci introduco la mano sinistra, nonostante la somiglianza fra le due mani. A livello molecolare, se mangio dello zucchero, che è costituito da molecole tutte della stessa chiralità, lo sento dolce e ne ricavo energia. Se provassi a mangiare l'enantiomero opposto dello zucchero, non sentirei il sapore dolce, non lo potrei utilizzare come fonte di energia, e probabilmente starei male per avvelenamento da una sostanza estranea. Quindi per tutte le sostanze chirali il mondo vivente ha fatto la sua scelta, utilizzando uno solo dei due enantiomeri. Avrebbe in principio potuto fare la scelta opposta, utilizzando gli amminoacidi D, gli zuccheri L, il DNA con elica di verso opposto, etc. Ma appunto avrebbe dovuto invertire la chiralità di tutti i composti, non solo di alcuni, altrimenti le interazioni fra i composti diversi non avrebbero più funzionato. Abbiamo qui un caso clamoroso di rottura della simmetria nel mondo naturale, di una scelta non giustificata da alcun principio, essendo la scelta opposta del tutto equivalente. Fu così che il violinista mancino di figura 8 divenne un "diverso". | ..... | ................................................
Fig. 7. La doppia elica
destrorsa del DNA B |
| .....................................................................
Fig. 8. Il violinista mancino
Immagine Left Handers Day | ........ | .................................................................................. Perché allora è stata fatta la scelta che conosciamo e non quella opposta? Questa domanda, che alcuni tendono a drammatizzare, ha in realtà una risposta banale. Se lanciamo una moneta, questa può cadere con uguale probabilità su una qualsiasi delle due facce, ma nel processo reale dovrà sceglierne una, testa o croce a caso, rompendo la simmetria; la simmetria sarebbe recuperata se facessimo molti lanci, perché allora i numeri di teste e croci sarebbero uguali. Così pure i viventi, dovendo scegliere fra due chiralità equivalenti, ma dovendo fare una scelta, ne hanno adottata una a caso. |
Il fatto poi che tutti i viventi presentano la stessa scelta, è uno dei tanti indizi che la vita sulla Terra è un fenomeno unitario, e che tutti gli esseri viventi derivano da un'unica origine, qualunque essa sia.
Gustavo Avitabile
.. Professore di Chimica macromolecolare (in pensione)
Universita' degli Studi Federico II di Napoli
Ultima Modifica 9 Anni 2 Mesi fa da Paolo.
Si prega Accesso a partecipare alla conversazione.
Tempo creazione pagina: 0.484 secondi